Предыдущие исследования в области нейробиологии неизменно демонстрировали глубокое влияние раннего жизненного опыта на работу мозга, особенно на формирование соединений, которые обеспечивают связь между нейронами (то есть синапсов). Было обнаружено, что влияние раннего жизненного опыта особенно сильно проявляется в так называемые сенситивные периоды (СФП) — периоды времени, в течение которых повышается пластичность мозга (то есть его способность формировать или реорганизовывать нейронные связи).
Экспериментальные данные свидетельствуют о том, что эти периоды повышенной пластичности мозга регулируются специализированными нейронами, которые выделяют ингибирующий нейромедиатор ГАМК (гамма-аминомасляную кислоту). Было обнаружено, что так называемые парвальбумин-позитивные (PV+) интернейроны играют центральную роль в развитии SPS, поскольку их постепенное включение в защитные структуры было связано с завершением этих периодов.
Исследователи из Университета Милана и Университета Хельсинки недавно провели исследование, изучающее влияние раннего приема широко назначаемого антидепрессанта флуоксетина (FLX) на регуляцию СФС у крыс. Их результаты, опубликованные в журнале Molecular Psychiatry, свидетельствуют о том, что воздействие флуоксетина во время вынашивания, беременности или грудного вскармливания может повлиять на развитие мозга и поведение крысят в более позднем возрасте.
«Опыт ранней жизни формирует нейронные сети, которые обладают повышенной пластичностью в так называемые «чувствительные периоды» (SPs)», — пишут Мария Тереза Галло, Анаис Виренке и их коллеги в своей статье. «SPs регулируются созреванием гамкергических PV+ интернейронов, которые со временем обволакиваются перинейрональными сетями (PNNS), модулируя закрытие SP. Кроме того, открытие и закрытие SP контролируется двумя различными группами генов, известными как «триггерные» и «тормозные».
Предыдущие исследования выявили две широкие группы генов, которые либо инициируют периоды повышенной пластичности мозга (т.е. SPS), либо закрывают их. Было обнаружено, что триггерные гены стимулируют открытие SPS, в то время как «тормозные» гены — их завершение.
Изменения в этих генетических механизмах были связаны с возникновением различных нервно-психических состояний. Основной целью недавней работы Галло, Виренке и их коллег было изучение возможного влияния внутриутробного и раннего воздействия препарата FLX на процессы, регулирующие открытие и закрытие СФС у крыс.
FLX является одним из наиболее часто назначаемых селективных ингибиторов обратного захвата серотонина (СИОЗС). Это фармацевтические препараты, которые могут лечить симптомы депрессии и других психических расстройств, повышая активность серотонина в головном мозге.
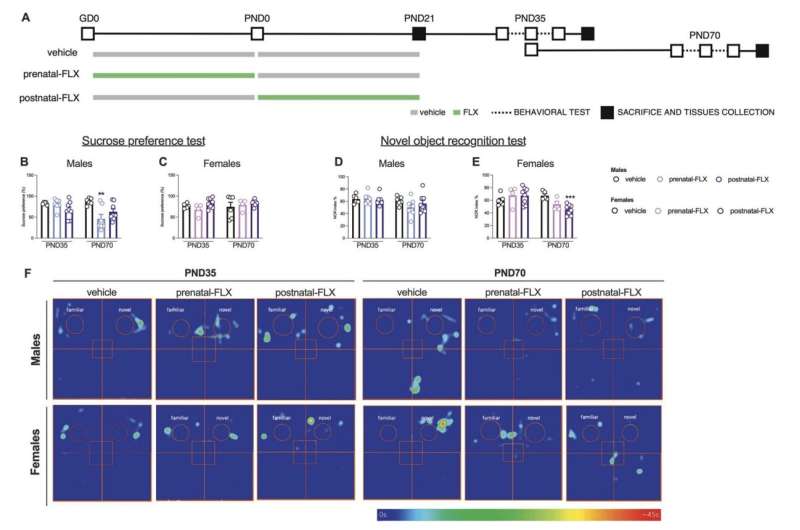
«Мы исследуем на крысах, связаны ли поведенческие фенотипы, наблюдаемые у взрослых, подвергшихся воздействию FLX во время беременности или грудного вскармливания (до 21-го послеродового дня), с изменениями в динамике SP», — пишут Галло, Виренке и их коллеги. «В соответствии с наблюдаемыми патологическими фенотипами взрослых, молекулярные результаты выявляют явные половые различия со значительными изменениями плотности PV+, доли PV+-клеток, окруженных PNN, а также экспрессии триггерных и тормозных генов в префронтальной коре на протяжении всей жизни и спинной гиппокамп.
Исследователи обнаружили, что воздействие FLX во время беременности (т.е. когда детеныши еще развивались в утробе матери) и грудного вскармливания оказывало различное влияние на сроки развития SPs в дальнейшей жизни. В частности, у самцов крыс, подвергшихся воздействию препарата, СПС открылись раньше обычного, в то время как у самок крыс, подвергшихся воздействию препарата, открылись позже обычного.
«Мы наблюдали самый сильный эффект в зубчатой извилине (DG) дорсального гиппокампа, с ожиданием открытия SP у мужчин с пренатальным FLX и задержкой у женщин с послеродовым FLX», — пишут авторы. «Мы предполагаем, что описанные здесь молекулярные мишени могут представлять собой полезные биомаркеры для идентификации людей с потенциально повышенной уязвимостью, и, соответственно, мы можем предположить, что стратегии (фармакологические или нет), направленные на коррекцию этих отклонений, могут быть полезны для предотвращения патологических проявлений».
Результаты, собранные этой исследовательской группой, указывают на возможность того, что употребление матерью FLX во время беременности может иметь долгосрочные последствия для развития мозга их потомства, потенциально увеличивая риск развития у них нервных или психических расстройств. Однако, чтобы иметь клиническое значение, они должны быть апробированы на людях.
В будущем результаты могут пролить дополнительный свет на нейронные и генетические механизмы, лежащие в основе развития мозга и установления важных нейронных связей. Это, в свою очередь, могло бы помочь в разработке новых протоколов или руководящих принципов, способствующих здоровому развитию мозга с самых ранних этапов жизни.
Эта статья, написанная для вас нашим автором Ингрид Фаделли, отредактированная Лизой Лок, а также проверенная по фактам и рецензируемая Робертом Иганом, — результат кропотливой человеческой работы. Мы полагаемся на таких читателей, как вы, в поддержании независимой научной журналистики. Если эта информация важна для вас, пожалуйста, подумайте о пожертвовании (особенно ежемесячном). В качестве благодарности вы получите аккаунт без рекламы.
Дополнительная информация: Мария Тереза Галло и соавт., От воздействия флуоксетина в раннем возрасте до изменений поведения в зависимости от пола на протяжении всей жизни: расшифровка динамики чувствительных периодов, Молекулярная психиатрия (2025). DOI: 10.1038/s41380-025-03223-6
Информация о журнале: Молекулярная психиатрия